medicatie
Het betreft hier zowel somatische medicatie als medicatie medicatie die gebruikt wordt in de behandeling van psychiatrische patiënten
Antipsychotische medicatie
- Gegevens
- Gemaakt op woensdag 09 januari 2019 14:12
- Laatst bijgewerkt op woensdag 09 januari 2019 14:12
- Gepubliceerd op woensdag 09 januari 2019 14:12
- Hits: 2391
De antipsychotische medicatie heeft vooral een zeer sterk kalmerend effect.
Mensen die het gebruiken kunnen het echter ook ervaren als versuffend. Het kan zijn dat het gebruik van de antipsychotische medicatie de onwerkelijke waarnemingen doet verminderen en zelfs doet verdwijnen. Dit effect treedt echter niet altijd op. De overtuiging dat men iemand anders is bijvoorbeeld "Jezus", hoeft niet weg te zijn en kan ondanks deze medicatie blijven bestaan. Mensen die tijdens een psychose een soort heldere waarnemingen en gedachten ervaren, ervaren in de regel wel dat deze ongewone helderheid sterk afneemt en zelfs verdwijnt en ervaren dit weer als een groot gemis.
Seroquel een Zwitsers zakmes?
- Gegevens
- Categorie: medicatie
- Gemaakt op vrijdag 04 januari 2019 22:21
- Laatst bijgewerkt op zaterdag 27 januari 2024 11:44
- Gepubliceerd op vrijdag 04 januari 2019 22:21
- Hits: 19913
Inhoud
- Een kleine geschiedenisles
- Waarom over Seroquel?
- Seroquel niet alleen voor patiënten met een psychose?
- Wat zeggen College ter Beoordeling van Geneesmiddelen en FDA over Seroquel?
- De medische "good practice" is kennelijk een andere dan wat het CBG "good practice" vindt
- En Astra Zenica keek en zag dat het geld binnenstroomde
- Wie wordt er beter van Seroquel?
- Sommige patiënten zien de voordelen van off-label gebruik
- Hoe ervaren patiënten Seroquel?
- Exitus infelix of exitus felix?
- Farmacologie
- Indicaties en gebruik
- Contra-indicaties
- Waarschuwingen
- Voorzorgsmaatregelen
- Bijwerkingen
- Symptomen en behandeling van te hoge dosering
- Dosering en toediening
- Toedieningsvormen
- Onderzoek
Een kleine geschiedenisles
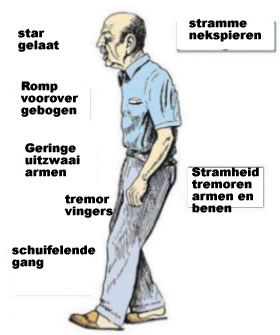 Toen ik begin jaren 80 in een psychiatrisch ziekenhuis kwam werken werd ik getroffen door de vele psychiatrische patiënten die stram en stijf door het parkachtige landschap van het ziekenhuis terrein schuifelden. Tijdens maaltijden en koffiedrinken, zag ik bij veel patiënten ernstige tremoren. Zonder morsen eten of drinken was vrijwel onmogelijk waardoor de kleding bij veel patiënten onder de vlekken zat. Bijna elke dag werd er wel een melding gedaan van een patiënt met
blikkramp of kaakklem
Toen ik begin jaren 80 in een psychiatrisch ziekenhuis kwam werken werd ik getroffen door de vele psychiatrische patiënten die stram en stijf door het parkachtige landschap van het ziekenhuis terrein schuifelden. Tijdens maaltijden en koffiedrinken, zag ik bij veel patiënten ernstige tremoren. Zonder morsen eten of drinken was vrijwel onmogelijk waardoor de kleding bij veel patiënten onder de vlekken zat. Bijna elke dag werd er wel een melding gedaan van een patiënt met
blikkramp of kaakklem
Vrijwel elke patiënt gebruikte laxerende medicatie. Dat alles kwam door de ongewenste bijwerkingen van de antipsychotische medicatie, leerde ik. Deze bijwerkingen worden extrapiramidale bijwerkingen en tardieve dyskinesie, genoemd.
Enkele van die antipsychotica waarvan sommige ook nu nog voorgeschreven worden, waren Largactil (Chloorpromazine, 1950) Haldol (haloperidol, 1958) Sordinol (Clopenthixol, 1961) en Cisordonol (Zuclopenthixol, 1978). Omdat deze antipsychotica tot de allereerste antipsychotische medicijnen, die ontwikkeld werden, horen, worden deze tegenwoordig de klassieke of typische antipsychotica genoemd. Niet zelden had een patiënt 2 tot drie verschillende antipsychotica, gecombineerd met antidepressiva en angstremmende medicatie. Er waren 2 manieren in zwang om iets aan deze ongewenste bijwerkingen te doen. De antipsychotische medicatie verhogen of Akineton een antiparkinson middel erbij voorschrijven. Door de verhoging van de antipsychotische medicatie konden bepaalde bijverschijnselen weliswaar verdwijnen maar uiteindelijk keerden de bijverschijnselen terug. Akineton heeft echter als bijverschijnsel tardieve dyskinesie. De psychotische onrust werd door de antipsychotica deels beteugeld maar wel ten koste van veel lichamelijk ongemak. Daar kwam bij dat deze antipsychotica een sterk vermindering van vitaliteitsgevoel veroorzaakten. Het was dan ook geen wonder dat er veel weerstand tegen deze medicatie was en dat patiënten zich vrijwel allemaal te pletter rookten en sloten koffie naar binnen werkten om zichzelf nog een beetje op te peppen. Vanaf midden jaren 80 kwam bij de artsen steeds meer het inzicht, dat het om de werking van medicatie beter in de hand te houden beter was te streven naar één antipsychoticum. De medicatie cocktails gingen steeds meer tot het verleden horen. In de jaren negentig, kwamen modernere antipsychotische middelen op de markt: de zogenaamde atypische antipsychotische medicatie waaronder Seroquel. De fabrikanten van deze atypische antipsychotische medicatie beweren dat deze medicatie niet of in veel mindere mate de de bijwerkingen heeft van de eerste antipsychotica, de zogenaamde klassieke antipsychotica. Het eerste en meest bekende atypische antipsychotische medicijn dat voorgeschreven werd, was Leponex(1990). daarna kwamen: Risperdal(1992), Zyprexa(1996), Seroquel(1997) en Abilify(2002). Patiënten die Seroquel krijgen voorgeschreven, hebben inderdaad minder last van extrapiramidale bijwerkingen en tardieve dyskinesie, wanneer wij hen vergelijken met patiënten die klassieke antipsychotica gebruiken.
Waarom een artikel over Seroquel?
| | |||||||
| |||||||
Daar moest ik het mijne van weten.
In het schouwspel dat zich vervolgens voltrok, verschenen een aantal spelers ten tonele: de hoofdrolspelers in volgorde van belangrijkheid, de patiënt de voorschrijvende arts, de fabrikant en Seroquel . Bijrollen zijn er is er voor het College ter Beoordeling van Geneesmiddelen, de FDA , de zorgverzekeraar en de onderzoeker.
Seroquel niet alleen voor patiënten met een psychose?
 Na enige studie van Seroquel kwam ik er achter dat Seroquel tegenwoordig ondanks
waarschuwingen,
door artsen, gebruikt wordt voor de behandeling van een breed scala psychiatrische stoornissen. Seroquel, wordt behalve bij psychotische stoornissen ook voorgeschreven bij patiënten met een bipolaire stoornis, bij patiënten met slaapstoornissen, een angststoornis, bij depressie, bij een periodieke explosieve stoornis. bij borderline persoonlijkheidsstoornissen, post traumatische stress stoornissen, delier, etc..
Na enige studie van Seroquel kwam ik er achter dat Seroquel tegenwoordig ondanks
waarschuwingen,
door artsen, gebruikt wordt voor de behandeling van een breed scala psychiatrische stoornissen. Seroquel, wordt behalve bij psychotische stoornissen ook voorgeschreven bij patiënten met een bipolaire stoornis, bij patiënten met slaapstoornissen, een angststoornis, bij depressie, bij een periodieke explosieve stoornis. bij borderline persoonlijkheidsstoornissen, post traumatische stress stoornissen, delier, etc..
Wat zeggen College ter Beoordeling van Geneesmiddelen en FDA over Seroquel?
Het College ter beoordeling van geneesmiddelen( CBG) acht Seroquel en langwerkende Seroquel geschikt voor de behandeling van psychotische aandoeningen die gekenmerkt worden door een gestoorde waarneming of ongebruikelijk verward denken, verlies van interesse in het leven en sterke of onaangepaste emoties. Het college acht Seroquel daarnaast geschikt voor de behandeling bipolaire stoornissen. Hoewel hier geen eenduidige onderzoeksresultaten over bekend zijn. De Federal Drug and Food Administration(FDA) in de V.S. acht Seroquel geschikt voor de behandeling van patiënten met een psychotische aandoening en een bipolaire stoornis. De FDA acht Seroquel niet geschikt voor de behandeling van een depressieve stoornis, slapeloosheid en angststoornissen. De FDA waarschuwt voor het gebruik van Seroquel bij ouderen met dementie vanwege een verhoogde kans op overlijden. De FDA raadt het af Seroquel te gebruiken bij vooral jongere patiënten die antidepressiva gebruiken en suïcidale gestes en overwegingen geuit hebben. Wanneer patiënten lijden aan leverstoornissen, hoge of lage bloeddruk, diabetes, epilepsie, cataract, een tekort aan witte bloedcellen, overgewicht, hoog cholesterol, cardiale, vasculaire, schildklierafwijkingen, in verwachting zijn en borstvoeding geven, moet de voorschrijvende arts speciale voorzorgsmiddelen in acht nemen wanneer hij de voordelen, groter acht dan de nadelen van het gebruik van SeroquelDe medische "good practice" is kennelijk een andere dan wat het CBG "good practice" vindt
Een medicijn voorschrijven voor een andere kwaal dan waarvoor het medicijn ontwikkeld is en goedgekeurd is door het College ter Beoordeling van Geneesmiddelen, wordt "off label voorschrijven", genoemd.Helemaal vreemd vond ik dat ook weer niet omdat ik in de wereld van de psychiatrie heb gezien dat psychiaters wel vaker medicijnen voorschrijven voor een andere kwaal dan waarvoor de medicijnen oorspronkelijk ontwikkeld werden. Een bekend voorbeeld is het voorschrijven van een anti-epileptisch middel bij een stemmingsstoornis. Bijvoorbeeld wanneer patiënten Lithium niet meer verdragen. Het menselijk brein is alle studie ten spijt, nog steeds een groot raadsel en psychiatrische ziekten zijn zo mogelijk een nog groter raadsel. Vaak zitten artsen met de handen in het haar omdat specifieke middelen voor een bepaalde ziekte zoals slapeloosheid, bij bepaald patiënten, niet helpen. Is het dan zo gek dat wanneer je ziet dat de bijwerking van in dit geval Seroquel slaperigheid veroorzaakt dat je Seroquel soms gebruikt wanneer de bestaande slaapmedicatie geen gewenst effect heeft. Het is daarom niet helemaal onbegrijpelijk, dat men er toe komt specifieke middelen voor een kwaal te gebruiken, waarvoor het middel eigenlijk niet ontwikkeld is.
De wens van artsen, iets te doen voor hun patiënten, is zo groot dat ondanks dat bekend is dat Seroquel leidt tot gewichtstoename en een verhoogde kans op diabetes, men zelfs Seroquel voorschrijft bij patiënten met een verhoogd risico op overgewicht, diabetes en hartproblemen. Dit wanneer men het voordeel dat men denkt te kunnen behalen hoger inschat.
In het kader van "do no harm"moet bij deze laatste handelswijze, natuurlijk een vraagteken geplaatst worden. Ook al komt het vaker voor dat medicijnen worden ingezet bij de behandeling van kwalen waarvoor zij niet bedoeld en niet ontwikkeld werden, toch kun je niet anders dan concluderen dat Seroquel wel voor een heel breed scala kwalen ingezet wordt door de hoogopgeleide psychiaters die zweven tussen willen genezen, wetenschappelijk en evidenced based handelen.

Psychiaters die niet zoals chirurgen een scalpel mogen hanteren, hebben dan toch een soort Zwitsers zakmes ter beschikking. Zo'n Zwitsers zakmes, waarmee je niet alleen kunt snijden maar ook zagen knippen, schroeven vijlen, blikken en flessen openen. Weliswaar krakkemikkig maar het werkt wel een beetje wanneer je handig bent. Wie weet helpt Seroquel wel krakkemikkig maar en hopelijk iets beter dan een placebo bij meerdere psychiatrische kwalen.
Natuurlijk hoeft het niet verkeerd te zijn, iets te proberen waarvan je de gevolgen niet helemaal kunt overzien. Zolang je dit maar doet in voortdurend overleg met de patiënt. Dat laatste vraagt echter meer dan de gebruikelijke controleafspraken. Ook al omdat de patiënten waar het hier om gaat, vaak niet goed kunnen verwoorden wat de effecten van medicijnen zijn.
| | ||
En Astra Zenica keek en zag dat het geld binnenstroomde
Of de Brits-Zweedse fabrikant Astra Zenica, die Seroquel op de eerste plaats ontwikkeld en onderzocht heeft ten behoeve van patiënten met een psychotische stoornis, er blij mee zou moeten zijn dat het middel nu breed wordt ingezet, is wetenschappelijk gezien de vraag. In de praktijk is de fabrikant er wel blij mee, gezien het extra geld dat hierdoor in het laatje komt. De omzet groeide in 2009 in de VS naar $7 miljard, grotendeels door off-label voorschrijven. Dit was het gevolg van de aanpassingen van Astra Zeneca, op de bijsluiter aan die andere toepassingen van het middel en een agressieve off label marketing campagne. Dit leidde er toe dat Seroquel zelfs aan kinderen en bejaarden werd voorgeschreven, voor indicaties die niet goedgekeurd waren door de Federal Drug and Food administration. In 2009 accepteerde Astra Zeneca hiervoor een forse financiële tik op de billen door een schikking te treffen met twee federale justitiële onderzoeken en klokkenluiders. Astra Zeneca meldde dat er op dat moment 14444 gerechtelijke procedures tegen het bedrijf gevoerd werden vanwege de aanbevolen toepassing, de voorgespiegelde werking en de nadelige bijwerkingen van Seroquel.Wie wordt er beter van Seroquel?
 Medicijnen - en ook Seroquel ontkomt hier niet aan - worden te vaak gezien als een panacee tegen alle kwalen. een toverelixer. Aan de ene kant heb je de altijd willen genezende en vaak off label voorschrijvende artsen met - de wie weet helpt Seroquel ook wel tegen "die kwaal"- mentaliteit. Aan de andere kant heb je Astra Zeneca de fabrikant die Seroquel ziet als een El Dorado waar onbeperkte rijkdom ontspruit en daarom niet schuwt nep informatie over de werking en onderzoek te verspreiden.
De sluitpost is de patiënt die het risico van de "onbedoelde"en het hopelijk voordeel van de "gewenste"bijwerkingen van Seroquel moet ondergaan.
Medicijnen - en ook Seroquel ontkomt hier niet aan - worden te vaak gezien als een panacee tegen alle kwalen. een toverelixer. Aan de ene kant heb je de altijd willen genezende en vaak off label voorschrijvende artsen met - de wie weet helpt Seroquel ook wel tegen "die kwaal"- mentaliteit. Aan de andere kant heb je Astra Zeneca de fabrikant die Seroquel ziet als een El Dorado waar onbeperkte rijkdom ontspruit en daarom niet schuwt nep informatie over de werking en onderzoek te verspreiden.
De sluitpost is de patiënt die het risico van de "onbedoelde"en het hopelijk voordeel van de "gewenste"bijwerkingen van Seroquel moet ondergaan.
Sommige patiënten zien de voordelen van off-label gebruik
Ook de consument van Seroquel valt iets te verwijten. Hoewel het recreatief vermogen. van Seroquel door medici en fabrikant betwijfeld wordt, denken sommige gebruikers hier anders over.Er zijn nogal wat artikelen geschreven over het "misbruik" van Seroquel. Er zijn gevallen bekend van mensen die symptomen voorwenden om recepten te verkrijgen voor Seroquel. Artsen van de Los Angeles County Jail rapporteerden een wijdverbreid intranasaal misbruik van Quetiapine. Zij waarschuwen voor gedetineerden die doen alsof ze psychotisch zijn om het middel te verkrijgen, en melden dat het middel een duidelijke straatwaarde heeft in het illegale circuit. Ook schijnt er in gevangenissen een levendige handel te zijn in Seroquel.Op straat staat het middel ook wel bekend als “baby heroïne” of “Suzie Q”. In gematigde doses werkt het als pepmiddel met een euforisch effect; hogere doses geven een versuft gevoel. Patiënten vergelijken de sederende werking met die van wiet en kunnen om die reden hoge doses gebruiken om de hele dag ‘stoned’ te kunnen zijn. Seroquel wordt ook misbruikt om te snuiven, zowel voor de onmiddellijke roes als het langer aanhoudende sederende effect. De onmiddellijke roes wordt een ‘kick’ genoemd en de intranasale toediening garandeert deze snelle werking. Voor een aantal gebruikers is deze ‘kick’ de belangrijkste reden om het middel te gebruiken, maar de grootste groep gebruikt het vanwege het angstremmende en sederende effect. Seroquel wordt ook gebruikt om bij te komen van andere drugs Er werd verslavingsgedrag gezien alsmede lichamelijke onttrekkingsverschijnselen.
Hoe ervaren patiënten Seroquel?
| | |||||||
| |||||||
Hoe kijken patiënten aan tegen de werkzaamheid van Seroquel?
Ondanks alle geld dat gestoken is in de ontwikkeling Seroquel als middel tegen psychotische stoornissen met weinig bijwerkingen, geven 27 gebruikers met een psychotische stoornis voor de werkzaamheid, slechts een score van 6,1. Patiënten waarbij Seroquel hoog scoort vanwege de werkzaamheid tegen hun psychose ervaren het probleem dat zij uiteindelijk met dit medicijn moeten stoppen omdat anders leverschade dreigt.
Patiënten die geen werkzaamheid ervaren bij hun psychose door Seroquel, klagen over het verslavende effect van Seroquel. Zij zijn bang nooit meer goed te kunnen slapen wanneer zij stoppen met de medicatie. Tegelijkertijd klagen zij dat zij vrijwel niet wakker te krijgen zijn wanneer zij door Seroquel slapen. Ook klagen zij over hun zucht naar suiker en de gewichtstoename die hierdoor plaatsvind.
zie:review
Patiënten die Seroquel gebruiken, klagen dat zij snel vermoeid zijn en 20 van de 24 uur tot bijna niets komen. Patiënten klagen ook over visuele vervormingen, moeite met wakker blijven en een depressief gevoel na ontwaken. Verder wordt er geklaagd over gewichtstoename, onrustige benen, onrustgevoelens, leverfunctie stoornissen.
Tegenover die nadelen van Seroquel worden zelden door de artsen effectieve middelen ter beschikking gesteld.
Patiënten met name de jongere patiënten die vertrouwd zijn met het gebruik van illegale drugs zijn daarom geneigd naast Seroquel speed tegen het vermoeide gevoel te gebruiken en cannabis tegen het neerslachtige negatieve gevoel. Zij willen af van dat inactieve vermoeide depressieve gevoel.
Artsen ontraden patiënten het gebruik van speed en cannabis tijdens de behandeling met medicatie.
In onderzoeken en adviezen aan patiënten legt men een relatie met de uitlokkende werking die cannabis en speed op het ontstaan of in stand houden van een psychose zouden hebben.
Mogelijk hebben cannabis gebruik en speed bij sommige patiënten een uitlokkende psychotische werking. Welke patiënten dat echter zijn is niet bekend. Cannabis is zeker niet nadelig bij alle patiënten die lijden aan een psychose. Kijken wij naar mensen die niet getroffen worden door een psychose en geen antipsychotica gebruiken maar wel speed en cannabis gebruiken, dan zien wij niet noodzakelijk een grote inactiviteit en/of incoherentie in hun dagelijkse leven. De meerderheid van de personen die cannabis en speed gebruiken leidt een relatief normaal werkzaam en sociaal leven. Bijzonder is, dat ondanks onvoldoende wetenschappelijk bewijs, dat met name de patiënten die klagen over slapeloosheid, ptss, ocs, bps en angststoornissen, seroquel, een waardering geven die varieert tussen 7,4 en 8. zie: reviews seroquel.
Exitus infelix of exitus felix?
Wellicht dat de aandachtige toeschouwer van het geschetste tafereel inmiddels vindt dat de patiënt helemaal niet de belangrijkste rol speelt. Je bent eerder geneigd de fabrikant van Seroquel als hoofdrolspeler en winnaar uit te roepen. Immers miljardenomzet, door propageren van off-label voorschrijven en het manipuleren van de kennis en onderzoek. De Seroquel en off-label voorschrijvende arts die pal voor zijn patiënt wil staan, heeft het moeilijk, Patiënten willen per se slapen en van hun angststoornis verlost worden. Fabrikanten bombarderen artsen met gegevens die in het voordeel van Seroquel spreken en laten gegevens die in het nadeel spreken achterwege. Wat kan de fabrikant een forse boete schelen. Hij heeft diepe zakken en bovendien heeft hij alle touwtjes in handen. Het schouwspel overziend blijft de patiënt met een psychose door en ondanks Seroquel, de goede bedoelingen van de voorschrijvend arts en de op winst beluste fabrikant, uiteindelijk de patiënt die geen andere keuze heeft dan het medicijn te slikken en de nadelen van de bijwerkingen te verdragen. Het is wrang te moeten constateren dat de fabrikant en gebruikers die Seroquel als een drug gebruiken, de enigen zijn die profiteren van Seroquel. Vreemd is het dat de patiënten die Seroquel off-label voorgeschreven krijgen voor bijvoorbeeld slaapproblemen Seroquel hoger waarderen dan de patiënten die lijden aan een psychose. Deze hogere waardering is echter geen vrijbrief om dan maar vrolijk door te gaan met off-label voorschrijven van Seroquel. Het zou zorgverzekeraars en CBG, sieren wanneer zij het off-label voorschrijven van seroquel niet zouden toestaan. Daar onafhankelijk onderzoek aan universiteiten dat gefinancierd wordt door de overheid, beschikt over te weinig middelen beschikt, zouden fabrikanten van farmaceutica alleen maar een middel op de markt mogen brengen wanneer zij jaarlijks een substantieel bedrag storten in een dergelijk onafhankelijk onderzoeksinstituut. De taken van een dergelijk instituut zouden moeten zijn te onderzoeken welk van de bestaande antipsychotica de beste antipsychotische bijwerking heeft gecombineerd met de minste bijwerkingen. Daar medicijnen helaas altijd ongewenste bijwerkingen hebben, dient een dergelijk instituut ook in te zetten op patiënten en artsen te voorzien van informatie en middelen die deze bijwerkingen doen verminderen. Het is te gek dat patiënten zelf naar middelen moeten zoeken, zoals speed, cannabis, nicotine en koffie. Voor degenen die meer willen weten over SeroquelVoor farmacologie, farmacokinetische eigenschappen, bijwerkingen, dosis, eliminatie, metabolisatie, en voorzorgsmaatregelen door aanpassing dosering en en toediening, lees verder.
Indicatie en gebruik:
Het College ter beoordeling van geneesmiddelen acht Seroquel tabletten en langwerkende Seroquel tabletten geschikt voor de behandeling van psychotische aandoeningen die gekenmerkt worden door een gestoorde waarneming of ongebruikelijk verward denken, verlies van interesse in het leven en sterke of onaangepaste emoties.Seroquel is daarnaast geschikt voor de behandeling bipolaire stoornissen. Hoewel hier geen eenduidige onderzoeksresultaten over bekend zijn. Voor degenen die meer willen weten over Seroquel Voor farmacologie, farmacokinetische eigenschappen, bijwerkingen, dosis, eliminatie, metabolisatie, en voorzorgsmaatregelen door aanpassing dosering en toediening, verwijs ik u naar: "Seroquel een zwitsers zakmes?" en de website "Evenwicht".
Farmacologie
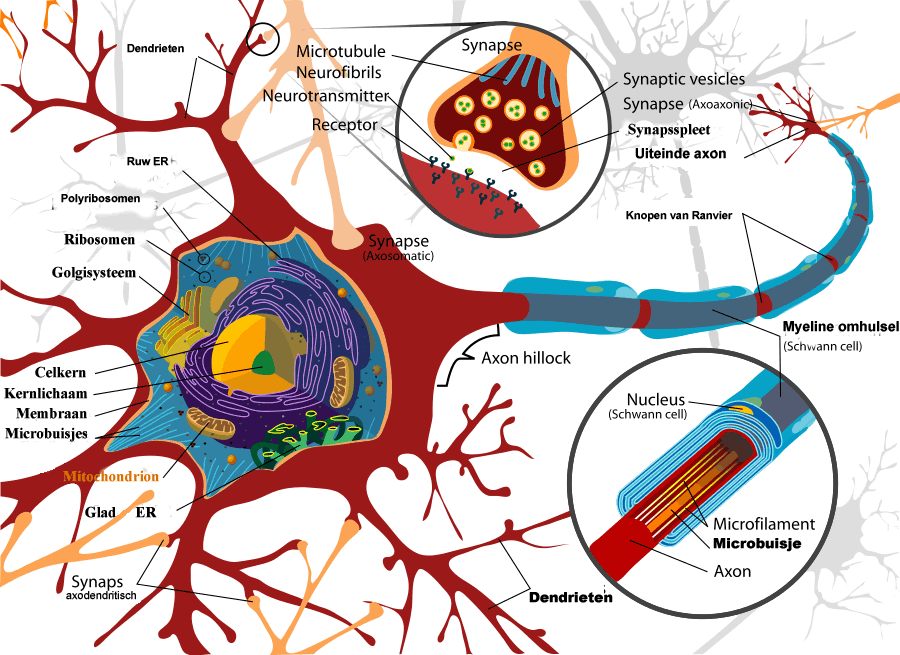
Het atypische antipsychoticum Seroquel, is een derivaat van dibenzothiazepine , en gaat in de neuronen van de hersenen een interactie aan met meerdere neurotransmittersneuron
Farmacokinetische eigenschappen
Dosis:Seroquel wordt via tabletten toegediend. De klinische dosis van Seroquel is gelijk voor mannen, vrouwen, rokers en niet rokers. Absorptie:
Na toediening van radioactief gemerkt Seroquel, bleek dat binnen een week, minder dan 5% onveranderd wordt uitgescheiden, waarvan (73%)in de urine en (21%) in faeces.
De belangrijkste plasma metabolieten in de mens bezitten geen significante farmacologische activiteit. De biologische beschikbaarheid van Seroquel wordt niet significant beïnvloed door gelijktijdige inname met voedsel.
De hoogste plasma concentratie Seroquel treedt op 2 uur na orale toediening. Eliminatie en Metabolisatie:
De halfwaardetijd van Seroquel is ongeveer 7 uur. Seroquel wordt voor ongeveer 83% aan plasma-eiwitten gebonden Seroquel wordt voornamelijk door de lever afgebroken. Voorzorg dosering en Toediening)
Voorzichtigheid moet in acht genomen worden bij patiënten met nier- en leverfunctiestoornissen
De gemiddelde plasmaklaring van Seroquel neemt met ongeveer 25% af bij patiënten met een ernstige nierfunctiestoornis (creatinineklaring lager dan 30 ml/min./1,73m2) alsook bij patiënten met een leverfunctiestoornis. werkzaamheid:
Seroquel bleek in korte termijn werkzaam bij de behandeling van schizofrenie. In drie onderzoeken van 6 weken werden patiënten die geclassificeerd waren als schizofreen, behandeld met Seroquel. In alle drie onderzoeken bleek Seroquel superieur aan het placebo. Het grootste effect werd bereik bij 300 mg. per dag.
Ondanks de halfwaardetijd van 7 uur, werkte Seroquel adequaat wanneer twee keer per dag werd toegediend. Dit gegeven werd ondersteund door de PET( positron emission tomography)scans waaruit bleek dat met Seroquel, de 5HT2 and D2 receptoren 12 uur volledig bezet bleven. In onderzoek met placebo's werden geen verschillen gevonden in het voorkomen van het voorkomen van het extra piramidaal syndroom. In hetzelfde onderzoek werd geen verband aangetoond tussen verhoging van de dosis Seroquel tot 750 mg. per dag en het voorkomen van het EPS, alsmede in de noodzaak van het gebruik van anticholinergica.
Anders dan veel andere antipsychotica veroorzaakt Seroquel geen blijvende stijgingen in prolactinespiegels, hetgeen als eigenschap van atypische antipsychotica wordt gezien. Er waren geen verschillen in prolactinespiegels over het gehele aanbevolen dosisbereik tussen meerdere vaste doses Seroquel en placebo bij het beëindigen van het klinisch onderzoek. Verhoogde prolactine spiegels worden in verband gebracht met bijwerkingen zoals galactorroe, amenorroe en impotentie.
Contraindicaties
Seroquel is mag niet verstrekt worden aan patiënten met een bekende overgevoeligheid voor dit medicijn of bestanddelen hiervan.Waarschuwingen
Neuroleptisch Malignant Syndroom (NMS):Het neuroleptisch malignant syndroom is een in potentie levensgevaarlijk syndroom dat gerapporteerd wordt in verband met het gebruik van antipsychotische medicatie, waaronder ook Seroquel. Bij het stellen van een diagnose is het belangrijk te letten op het gelijktijdig voorkomen van een ernstige medische ziekte zoals bijvoorbeeld longontsteking en onbehandelde of inadequaat behandelde extrapiramidale verschijnselen en symptomen. Andere belangrijke overwegingen waarbij tijdens de diagnose rekening mee ghouden moet worden zijn centrale anticholinerge toxiciteit, koortsaanvallen, door medicijnen veroorzaakte koorts en pathologie van het centraal zenuwsysteem. Bij de behandeling van NMS moet antipsychotische medicatie onmiddellijk gestaakt worden, dus ook Seroquel, alsmede andere medicijnen die niet essentieel zijn bij de behandeling van NMS. of toevallig andere aanwezige ernstige medische problematiek.
Na een doorgemaakt NMS moet, wanneer de antipsychotische medicatie weer noodzakelijk is de opbouw hiervan zeer zorgvuldig met de nodige voorzorgsmaatregelen geschieden daar het NMS opnieuw op kan treden. Tardieve Dyskinesie:
Alhoewel patiënten bij het gebruik van Seroquel een Kleinere kans hebben, tardieve dyskinesie te ontwikkelen, dan bij conventionele antipsychotica, is de kans zeer zeker aanwezig.
Ouderen met name vrouwen lopen het grootste risico op het ontwikkelen van tardieve dyskinesie.
Het is moeilijk een voorspelling te doen over het risico op tardieve dyskinesie.
Hiermee rekening houdend, dient Seroquel zodanig te worden voorgeschreven dat de kans op het voorkomen van tardieve dyskinesie zo klein mogelijk blijft.
Wanneer desondanks tekenen van tardieve dyskinesie optreden moet serieus overwogen worden de behandeling met Seroquel te staken..
Voorzorgsmaatregelen:
Lage bloeddruk en flauwvallen:Net zoals alle medicijnen die een sterke blokkade van de adrenerge receptoren veroorzaken, kan Seroquel duizeligheid door lage bloeddruk veroorzaken en soms flauwvallen. Met name tijdens het instellen op Seroquel.
Flauwvallen komt bij 1% (22/2162) van de met Seroquel behandelde patiënten voor.
Bij de patiënten die met een placebo behandeld werden kwam 0% (0/206) flauwvallen voor.
Bij patiënten die met een controle medicijn behandeld werden kwam 0.5% (2/420) flauwvallen voor. Het risico op flauwvallen kan verlaagd worden door een geleidelijke instelling op Seroquel. Dosering en toediening:
Grotere waakzaamheid moet in acht genomen worden wanneer men patiënten met hart en vaarproblemen met Seroquel behandeld. (b.v. patiënten die in het verleden een hartinfarct hadden of bij patiënten met een stoornis in de bloedvoorziening van de hartspier, hartfalen, geleidingsstoornissen, hartritmestoornissen, aandoeningen in de bloedvaten van de hersenen of andere toestanden die voorafgaan aan lage bloeddruk zoals uitdroging, tekort aan bloed en behandeling met bloeddrukverlagende medicijnen. Cataract:
De ontwikkeling van ooglens vertroebeling(staar) wordt in verband gebracht met het gebruik gebruik van Seroquel Deze observatie werd gedaan wanneer honden 4 keer de menselijke dosis toegediend kregen en bij patiënten die langdurig behandeld werden met Seroquel. een oorzakelijk verband kon echter niet vastgesteld worden. De mogelijkheid van veranderingen in het zicht zoals bijvoorbeeld dubbelzien bij langdurig gebruik van Seroquel kan nog niet uitgesloten worden. Daarom wordt bij het starten met Seroquel speetlamponderzoek aanbevolenen met tussentijdse herhalingen om de zes maanden. Wanneer er duidelijke veranderingen aan de ooglens worden waargenomen dient het stoppen van de Seroquel medicatie overwogen te worden. epileptische toevallen:
Uit onderzoek bij patiënten die seroquel kregen toegediend bleek er geen verschil met patiënten die een placebo kregen toegediend. Net zoals bij ander antipsychotica zijn er bedenkingen bij het toedienen van Seroquel wanneer patiënten in het verleden epileptische insulten doormaakten of een verhoogde kans hebben op epilepsie. Hypothyroidie
Onderzoek bij patiënten, toonde in de eerste 4 weken van toediening van Seroquel, een sterk verband aan met een verlaging van het schildklierhormoon. Bij 42% van de patiënten ging het om een verlaging van 30%. Bij 7% van de patiënten ging het zelfs om een verlaging van 50%:
Deze vermindering bleef of werd zelfs groter wanneer doorgegaan werd met toediening van Seroquel.
Deze verlagingen konden niet in verband gebracht worden met het minder of slechter werken van de schildklier. Routinematige monitoring van de schildklier functie in quetiapine behandelde patiënten zonder voorgeschiedenis van de ziekte van de schildklier wordt niet aanbevolen.
Bij 0.4% (10/2386) van de patiënten die behandeld werden met Seroquel werden blijvende verhogingen van TSH waargenomen. en bij 0.25% van de patiënten was een behandeling met een vervangende TSH noodzakelijk. Te hoge cholesterol en triglyceriden spiegel:
In kortlopende onderzoek bleek bij gebruik van Seroquel een verhoging van 11% cholesterol en van 17% trigliceriden. Patiënten die een placebo ontvingen bleken juist een verlaging van beide waardes te vertonen. De verhoging van cholesterol en triglyceriden ging niet gepaard met toename in gewicht. Transaminase: verhogingen:
Voordat Seroquel op de markt beschikbaar kwam als antipsychoticum, werd het in verband gebracht met het veroorzaken van een verhoging van de leverenzymes ALAT Van de 1892 patiënten die met Seroquel behandeld werden hadden 133 patiënten een dermate verhoogde ALAT dat gedacht werd aan behandeling. Echter geen van deze patiënten vertoonde symptomatologie die wees op een leveraandoening.
Het merendeel van de verhoogde enzymwaardes was alleen zichtbaar de eerste 2 maanden van de behandeling met Seroquel.
Van de 40 patiënten die stopten met Seroquel, bleven de enzymespiegels verhoogd.
Wanneer patiënten bekend zijn met een aandoening aan de lever moet voorzichtigheid betracht worden bij het starten met Seroquel. De transaminase spiegels moeten blijvend onderzocht worden. Hyperprolactinemie::
Uit dierstudies bleek een toename van prolactine bij toediening van Seroquel. Het verband bij mensen is minder duidelijk. Daar 1/3 van de borsttumoren bij vrouwen verband houdt met verhoogde prolactine moet vervolgonderzoek plaatsvinden wanneer de menstruatie uitblijft, of juist hevig bloedverlies plaatsvindt en wanneer er melkafscheiding wordt waargenomen Gewichtstoename:
Serqouel wordt net als andere atypisch antipsychotica zoals Leponex en Zyprexa in verband gebracht met gewichtstoename Na 4 tot 8 weken bleek een gewichtstoename van2.1 kg, Na 18-26 weken, 3.5 kg, en na 1 jaar, 5.6 kg. Effect op Cognitieve prestaties en beweging:
Slaperigheid wordt vaak gerapporteerd als een ongewenste bijwerking bij patiënten die Seroquel gebruiken. Met name in de opbouwperiode. Daar Seroquel een bewustzijns verlagend effect heeft en ook bewegingen vertraagd wordt het besturen van een motorvoertuig en het bedienen van een gevaarlijke machine afgeraden. Antibraak effect: Seroquel is een dopamine antagonist. In overeenstemming daarmee remt of onderdrukt Seroquel braakneigingen. Een dergelijk effect maskeert tekenen van vergiftiging door een overdosis van welk medicijn dan ook. Het maskeert ook symptomen van hersentumoren of verstopping van het darmkanaal. Regulatie lichaamstemperatuur:
Het is bekend dat antipsychotica de regulatie van de lichaamstemperatuur kunnen verstoren. Tot nu toe werd dit niet bij Seroquel gerapporteerd. Echter is het noodzakelijk aangepaste zorg te verlenen bij patiënten die Seroquel gebruiken wanneer zij blootgesteld worden aan extreme hitte waardoor hun kerntemperatuur omhoog kan gaan en kans maken op uitdroging. zeker wanneer zij gelijktijdig medicatie krijgen met anticholinerge effecten. Suicide:
psychotische patiënte hebben een verhoogd risico op suïcide of op een poging tot suïcide. Samen met antipsychotische medicatie dient er altijd een risico inschatting gemaakt worden en een plan om dit risico te beperken.
Interactie met andere medicijnen:
Omdat Seroquel invloed uitoefent op het centraal zenuwstelsel moet extra voorzichtig te werk gegaan wordt wanneer er ook andere medicijnen gebruikt worden die invloed hebben op het centraal zenuwstelsel. Seroquel versterkt de effecten van alcohol Seroquel. Het bewustzijn wordt verlaagd waardoor reactiesnelheid en de bewegingen worden hierdoor vertraagdWanneer Seroquel gebruikt worden dient men geen alcoholische dranken te gebruiken.
Vanwege de bloeddruk verlagende werking van Seroquel kan Seroquel de werking versterken van middelen die gebruikt worden tegen hoge bloeddruk.
Zoals bij in vitro onderzoek gebleken is Seroquel een dopamine antagonist. Seroquel kan daardoor de werking van levodopa en andere dopamine bevorderende middelen verlagen. CYP3A4 is het belangrijkste enzym dat verantwoordelijk is voor de metabolisatie regulering van cytochrome P450- van Seroquel. Gelijktijdige toediening van verbindingen (zoals ketoconazol, erytromycine, claritromycine, diltiazam, verapamil of nefazodon) die CYP3A4 remmen, kan dus de concentratie Seroquel verhogen. Voorzichtigheid is geboden bij de gelijktijdige toediening van Seroquel met krachtige CYP3A4 verlagende middelen zoals ketoconazole of erythromycin. gelijktijdige toediening Seroquel met phenytoin (een middel dat afgeleid is van metabolisatie bevorderende enzymen) veroorzaakt een vijfvoudige verlaging van Seroquel in het bloed. Een verhoging van de dosis Seroquel is dan noodzakelijk om de kans op een een psychose te verlagen. Ook carbamazepine, barbituraten, rifampicin) hebben een dergelijk effect Wanneer phenytoine wordt gestaakt kan het noodzakelijk zijn de dosis Seroquel te verlagen. Gelijktijdige toediening van thioridazine (200 mg 2xdaags) met Seroquel Seroquel (300 mg 2xdaags), zorgt voor afname van Seroquel met 65%. Bij gelijktijdige toediening van fluoxetine (60 mg per dag), imipramine (75 mg 2xdaags), haloperidol (7.5 mg 2xdaags), and risperidone (3 mg 2xdaags) heeft geen invloed op de farmacokinetiek van Seroquel. De farmacokinetiek van Lithium verandert niet bij gelijktijdige toediening met Seroquel. Seroquel beïnvloedt niet het lever enzym dat betrokken is bij metabolisatie van antipyrine. Gebruik bij 65+:
Bij 13 van de 36 65 plussers met een psychotische stoornis bleek tijdens een onderzoek dat Seroquel langzamer uit het bloedplasma te verdwijnt. Daar komt bij dat bij deze groep vaker problemen zijn met lever, nieren, het centraal zenuwstelse, bloedvaten en hart. Bijgevolg is de kans groter dat deze groep nog andere medicijnen gebruikt dan een antipsychoticum.
Het is noodzakelijk de dosis Seroquel bij 65 plussers uiterst zorgvuldig zorgvuldig te doseren. Gebruik bij kinderen en adolescenten
De veiligheid en werkzaamheid van Seroquel bij kinderen onder de 18 is nog onvoldoende door de fabrikant onderzocht.
Uit andere onderzoeken is gebleken dat Seroquel werkt en afgezien van bijwerkingen zoals gewichtstoename en toename van triglyceriden wel veilig lijkt bij kinderen.
In de meeste landen is Seroquel geen geregistreerd medicijn voor kinderen.
Een medische behandeling bestaat vaak uit een afweging van de voordelen tegen de nadelen. Wanneer een arts vastgesteld heeft dat een geregistreerde en goedgekeurde behandeling niet werkt en inschat dat Seroquel bij de behandeling van kinderen met een psychotische stoornis, een bipolaire stoornis zelfs een slaapstoornis zou kunnen werken, zal hij toch overwegen Seroquel voor te schrijven. De voordelen daarvan moeten dan wel opwegen tegen de potentiële risico's (bijv. de bijwerkingen). In Nederland is dat bij kinderen tussen 12 en 18 jaar zal voorschrijven. Gebruik bij patiënten met leverfunctie en nierstoornissen
Seroquel wordt voor een belangrijk deel door de lever afgebroken. Er is weinig ervaring met de behandeling van patiënten die een bijkomende leverfunctiestoornis en of nierstoornis hebben Ook hier geldt bij het titreren van de medicatie, meer geleidelijkheid en kleinere stappen. Gebruik bij zwangeschap
Wanneer patiënten zwanger raken of overwegen zwanger te raken, tijdens een behandeling met Seroquel, dienen zij hun arts te raadplegen.
De veiligheid van Seroquel tijdens zwangerschap is niet vastgesteld. Bij dierproeven zijn er aanwijzingen van schadelijkheid. Farmacologisch effect: Na blootstelling in het 3e trimester van de zwangerschap is er bij pasgeborenen kans op extrapiramidale symptomen en ontwenningsverschijnselen (tremor, hypertonie, hypotonie, agitatie, slaperigheid, ademnood, voedingsstoornis). Hier geldt zeker dat de voordelen van gebruik de de risico's van gezondheidsschade voor het ongeboren kind, verre dienen te overstijgen.
Het dient vrouwen ontraden te worden Seroquel te gebruiken tijdens de borstvoeding.
Ongewenste bijwerkingen
Bij een onderzoeksgroep met patiënten die Seroquel kregen toegediend bleek in deze groep een 5% hoger voorkomen van duizeligheid, slaperigheid, droge mond, lage bloeddruk gerelateerd aan liggen zitten en staan en verhoogde leverenzymen in het bloed vergeleken met patiënten die een placebo toegediend kregen.Bijwerkingen die in verband worden gebracht met het staken van Seroquel:
3.9% van de 510 patiënten die met Seroquel werden behandeld en 2,9% van de 206 patiënten die met een placebo werden behandeld ontwikkelden slaperigheid wanneer hun medicatie en vermeende medicatie gestaakt werd.Lage bloeddruk bij een houdingsverandering van liggen naar zitten en of van zitten naar staan en een versnelde onregelmatige hartslag kwam bij 1 % van de patiënten voor wanneer Seroquel gestaakt werd en bij 0,5 % wanneer het placebo gestaakt werd. 5% Van 1710 patiënten die met Seroquel behandeld werden, stopten na een ervaring met een bijwerking.
Slaperigheid was bij 24 patiënten de reden om te stoppen met Seroquel.
17 Patiënten stopten met Seroquel na problemen gerelateerd aan hart en vaten: duizeligheid door lage bloeddruk wanneer van een zittende naar een staande houding werd overgegaan en hartritmestoornissen.
16 Patiënten stopten met Seroquel na verhoogde leverenzymen.
4 patiënten stopten met Seroquel nadat zij leukopenie ontwikkelden. 2 van deze patiënten hadden een dergelijk laag aantal neutrofiele granulocyten in hun bloed dat hun aantal niet vastgesteld kon worden.
Bij 2 patiënten was was stoppen met Seroquel noodzakelijk vanwege de verdenking van het neuroleptisch malignant syndroom.
Bijwerkingen in een placebo-gecontroleerd onderzoek bij patiënten:
Het gaat om bijwerkingen in de eerste 6 weken van behandeling mbij patiënten met 150 mg Seroquel of meer per dag, Te zien is dat de bijwerkingen met Seroquel vaker optreden dan bij patiënten die een placebo toegediend kregen.| Table 1: gerapporteerde bijwerkingen bij ten minste 1% van de patiënten die met Seroquel werden behandeld.(doses >= 150 mg/dag) a | ||
| Deel lichaamssysteem | Percentage individuen met ongewenste bijwerkingen * | |
| Seroquel (n = 449) | Placebo (n = 202) | |
| Hoofdpijn | 20 | 17 |
| Buikpijn | 4 | 1 |
| Rugpijn | 2 | 1 |
| Koorts | 2 | 1 |
| Zenuw systeem | ||
| Slaperigheid | 18 | 11 |
| Duizeligheid | 10 | 4 |
| Spijsvertering | ||
| Verstopping | 9 | 5 |
| Droge mond | 7 | 2 |
| Dyspepsie | 6 | 2 |
| Verhoogde Gamma glutamyl transpeptidase | 2 | 1 |
| Hart en bloedvaten | ||
| Lage bloeddruk bij veranderen houding | 8 | 2 |
| Hartritmestoornissen | 7 | 5 |
| Hartkloppingen | 1 | 0 |
| Stofwisselings en eetstoornissen | ||
| Verhoogde SGPT | 7 | 2 |
| Verhoogde SCOT | 4 | 1 |
| Gewichtstoename | 2 | 0 |
| Endocrien systeem | ||
| Verlaagde schildklierwerking | 1 | 0 |
| Huid | ||
| Uitslag | 4 | 3 |
| Luchtwegen | ||
| Neusslijmvliesontstekingen | 3 | 1 |
| Het bloed- en lymfevatensysteem | ||
| tekort aan witte bloedlichamen | 2 | 0 |
| Horen, Zien,tast, reuk, evenwicht,smaak | ||
| Oorpijn | 1 | 0 |
| *Individuen kunnen meer dan een bijwerking vertoond hebben. | ||
Net als andere antipsychotica wordt Seroquel in verband gebracht met gewichtstoename bij het begin van de behandeling. (Na 6 en meer weken). vergeleken met een placebo is de gewichtstoename bij Seroquel gebruik gemiddeld 2,3kg en bij een placebo een te verwaarlozen 0,1 kg.
toevallen:
Af en toe wordt er melding gedaan van het voorkomen van epileptische insulten na het starten van Seroquel. Hierbij moet aangetekend worden dat het aantal insulten niet groter is bij de groep patiënten die een placebo ontving. Het neuroleptisch malignant syndroom:
Ook bij het gebruik van Seroquel bestaat er een kans zij het een kleine kans op het neuroleptisch malignant syndroom. Vitale signalen:
Seroquel blokkeert alfa-1 adrenerge receptoren en heeft net zoals ander antipsychotica met deze werking een ongunstige werking op hartritmestoornissen, duizeligheid en flauwvallen bij het uit bed komen of uit een stoel opstaan. Ook hier komen deze symptomen significant vaker voor bij Seroquel gebruikers vergeleken met placebogebruikers.
Zie voorzorgsmaatregelenIn Veranderingen gemeten in het laboratorium:
Voorbijgaande tekorten in de witte bloedlichaampjes en neutrofiele granulocyten, werden gemeten bij patiënten die Seroquel gebruikten. Soms werd er een tekort aan eosinofiele granulocyten geobserveerd. Ernstige blijvend tekort aan neutrofiele granulocyten werd niet geobserveerd. Verhogingen van bloedwaarden zonder lichamelijke symptomen
Ondanks dat er in gestold bloeplasma verhoogde transaminases [SGOT (AST), SGPT (ALAT)] of gamma-GT werden geobserveerd bij sommige patiënten die Seroquel kregen toegediend, leidde dit niet tot lichamelijke symptomen en bleken deze ook weer af te nemen naar een normaal niveau wanneer de Seroquel therapie werd voortgezet. Kleine verhogingen serumtriglyceriden- niveaus en cholesterol, gemeten in niet-nuchtere toestand, zijn waargenomen tijdens de behandeling met Seroquel. Behandeling met Seroquel in de eerste 4 weken werd in verband gebracht met dosis-gerelateerde verlagingen van het schildklierhormoon T4. Na doorgaan met Seroquel behandeling werd geen verdere verlaging meer waargenomen. In alle gemeten individuen met verlaging bleek het hormoon peil T4 zich te herstellen na het staken van de seroquel medicatie. Veranderingen in meting van het electro cardiogram
Er werde geen ECG verschillen gevonden tussen patiënten die Seroquel kregen toegediend en patiënten die een placebo gebruikten.
Wel werd er een klein verschil gemeten in hartritmestoornissen. Bij patiënten die Seroquel kregen toegediend was er een iets grotere verdenking van een hartritmestoornis dan bij patiënten die een placebo kregen toegediend. Extrapyramidale Symptomen (EPS)
Tabel 2 vermeldt de percentages van een kortdurende onderzoek bij 6 groepen patiënten n= 50 die een extrapiramidaal syndroom ontwikkelden voortgekomen uit behandeling met 5 verschillende doses Seroquel en en placebo. Het betrof ongevraagde klachten over parkinsonisme (extrapiramidaal syndroom, acathisie, spierspanningen/krampen, tremoren, Weerstand gevoeld bij het bewegen van een gewricht over de gehele beweging als een tandwiel aanvoelend.
| Tabel 2: Extrapyramidale Symptomen na behandeling,
op grond van gemelde klachten, Simpson Schaal, incidentie gebruik
anticholinergica.
|
|||||||
| Klachten en gebruik antichoninergica; | placebo | Seroquel | |||||
|---|---|---|---|---|---|---|---|
| 75 mg | 150 mg | 300 mg | 600 mg | 750 mg | |||
| spontaan gemelde klachten van Parkinsonsymptomen* | 10% | 6% | 4% | 4% | 8% | 4% | |
| spontaan gemelde klachten van bewegingsonrust | 8% | 2% | 2% | 0% | 0% | 2% | |
| Simpson Schaal | -0.6 | -1.0 | -1.2 | -1.6 | -1.8 | -1.8 | |
| Gebruik van anticholinergica | 14% | 11% | 10% | 8% | 12% | 11% | |
| *Patiënten kunnen meer dan een bijwerking ervaren. | |||||||
Symptomen en behandeling van overdosering
Er is weinig onderzoek gedaan naar overdosering. Bekend is dat er doseringen tot wel 10 gram zijn genomen waarvan de patiënte zonder gevolg herstelden, Over het algemeen was de mate van symptomen zoals versuftheid, verdoving, hartritmestoring en lage bloeddruk ernstiger, BehandelingEr is geen antidotum(tegengif) voor Seroquel. Wanneer er sprake is van intoxicatie moet de mogelijkheid overwogen van andere betrokken medicijnen of drugs. Verder moet men overgaan tot intensive care, zorgen voor hartbewaking en toevoer van zuurstof. intensive medische zorg en toezicht moet voortgezet worden tot het herstel van de patiënt.
Dosering en wijze van toediening
Het instellen van Seroquel duurt 4 tot 7 dagen. de begindosering van Seroquel is 25 mg 2xd, wanneer verhoging plaats vindt gebeurt dit met 25-50 mg 2xd zolang dit verdragen wordt gaat men hiermee door tot een dosis van 300 mg per dag. as tolerated, to a target dose of 300 mg/day gegeven in twee doseringen Afhankelijk van het gedrag van de patiënt vindt verdere aanpassing van de dosering plaats. De tussenliggende periode van een aanpassing van de dosering is minimaal 2 dagen. Een stabiele Seroquel spiegel houdt bij de gemiddelde patiënt ongeveer anderhalve dag aan.Wanneer aanpassingen van dosering noodzakelijk zijn gebeurdt dit door de dosis in stappen van 2xd 25 mg, te verhogen of te verlagen. Seroquel kan met of zonder eten gegeven worden. De werkzame dosis ligt normaal gesproken tussen de 300-600mg Seroquel. However, Enkele patiënten kunnen toe met 150 mg per dag. De veiligheid van meer dan 800 mg per dag is niet onderzocht. De noodzaak om verder te behandelen met een medicijn dat EPS kan veroorzaken moet voortdurend onderzocht worden Ouderen::
De nodige zorgvuldigheid moet worden betracht wanneer 65 plussers met Seroquel worden behandeld omdat onvoldoende duidelijk is hoe deze leeftijdsgroep op deze medicatie reageert. temeer daar ouderen vaak meer dan een medicijn gebruiken. Waarschijnlijk kan de dosis Seroquel bij ouderen lager zijn dan bij volwassenen onder de 65. Leverstoornissen
Seroquel wordt voor het grootste deel afgebroken door de lever. Therefore, Wanneer patiënten een leverfunctiestoornis hebben, dient behandeling met Seroquel met de grootst mogelijke voorzichtigheid te gebeuren. Het instellen van Seroquel dient langzamer en met kleiere stappen te gebeuren. . Nier stoornis::
Onderzoek met patiënten met een nierfunctiestoornis en tevens Seroquel gebruiken is niet gedaan. Ook bij een nierfunctiestoornis geldt dus dat voorzichtigheid geboden is.
Voorhanden zijnde Doseringen
 Seroquel dient bewaart te worden bij 15 - 30?C.
Seroquel dient bewaart te worden bij 15 - 30?C.
Onderzoek
Voor elk medicijn en ook Seroquel is het belangrijk te kijken naar het onderzoek wat er gedaan is en wat het heeft opgeleverd. Het onderzoek naar vele medicijnen en ook het onderzoek naar Seroquel is gebrekkig te noemen. De resultaten van dit onderzoek kunnen vertekend zijn, mogelijk als gevolg van de invloed van farmaceutische bedrijven. Bedenk ook hoe Astra Zeneca onderzoeken naar Seroquel verdoezeld en vervormd heeft met als doel het marktaandeel te vergroten en artsen aan te moedigen het middel off label voor te schrijven. Medisch onderzoeken naar de werking van medicijnen bij patiënten worden gekenmerkt door hoge uitvalcijfers van deelnemende patiënten bij deze onderzoeken. Uitvallende deelnemers staan voor ontbrekende gegevens. Na afloop van deze onderzoeken kun je geen betrouwbare en valide conclusies geven over de effectiviteit van Seroquel of wat de nadelige bijwerkingen zijn.websites
Info quetiapine voor artsenSeroquel info voor patiënten
website the drug classroom
Duff Wilson AstraZeneca Pays Millions to Settle Seroquel Cases, The New York Times (29 oktober 2009)
College ter beoordeling van geneesmiddelen: zie geneesmiddelen informatiebank
RIVM rapport 370050001/2007 Off-label gebruik van geneesmiddelen, Transparantie gewenst 2007
Lees de ervaringen en meningen over Seroquel(quetiapine) van 22 patiënten met een psychotische stoornis
Heroïne
- Gegevens
- Gemaakt op zondag 03 juli 2016 00:49
- Laatst bijgewerkt op vrijdag 23 augustus 2019 11:58
- Gepubliceerd op zondag 03 juli 2016 00:49
- Hits: 9398
Heroïneverslaving(afhankelijkheid) Symptomen en effecten
Heroïne (C21H23NO5), stofnaam diacetylmorfine,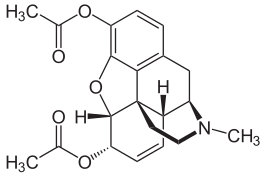 is een geurloos, bitter smakend opiaat. Het is de 3,6-diacetylester van morfine. De stof komt voor als een wit poeder of bruine, stugge kristallen, die zeer goed oplosbaar zijn in water.
is een geurloos, bitter smakend opiaat. Het is de 3,6-diacetylester van morfine. De stof komt voor als een wit poeder of bruine, stugge kristallen, die zeer goed oplosbaar zijn in water.

Heroïne wordt gemaakt van morfine, een natuurlijke stof die wordt verkregen uit het ingedroogde melksap(ruwe opium) van de opiumpapaver of slaapbol (Papaver somniferum.
 Het Duitse Bayer bracht diacetylmorphine als een zelfzorgmedicijn op de markt en registreerde in 1898 de merknaam "heroïne".
Het Duitse Bayer bracht diacetylmorphine als een zelfzorgmedicijn op de markt en registreerde in 1898 de merknaam "heroïne".
Hoe werkt heroïne?
Heroïne kan op meerdere manieren toegediend worden:- Intraveneus: directe injectie
in een ader met behulp van
een spuit en naald biedt
de snelste werking en de
grootste intensiteit. Ongeveer 10% van gebruikers injecteert heroïne.
Lees: Hoe heroïne intraveneus injecteren?
- Roken(chinezen): inademing mondeling via zilverpapier.
of door een pijp: 90% van de gebruikers.
- Snuiven: rechtstreeks via de neus, eventueel met behulp van een rietje
De effecten treden binnen tien tot vijftien minuten op.
In de hersenen wordt Heroïne omgezet in morfine en bindt zich snel aan opiaatreceptoren.
Heroïne verworven op de straat wordt versneden, of gemengd met andere drugs of met witte stoffen zoals suiker, zetmeel, of melkpoeder.
Wordt je verslaafd na eerste gebruik van heroïne?
Van heroïne wordt gezegd dat je verslaafd bent en niet meer zonder kunt na het eerste gebruik. Deze stelling is hoogstwaarschijnlijk niet meer waar dan dat je verslaafd wordt aan alcohol of tabak na eerste gebruik.In de VS documenteerde een team onder leiding van sociologe en epidemiologe Lee Robins veteranen die in Vietnam verslaafd waren geraakt aan heroïne, die bij terugkeer 19 van de 20 keer spontaan en zonder problemen stopten met heroïnegebruik.
Een van de kernbevindingen van het inmiddels opgeheven centrum v voor drugsonderzoek CEDRO in Amsterdam was, dat veruit het meeste druggebruik vanzelf stopt als de levensstijl van de gebruiker verandert.
Een waarschuwing is op zijn plaats:
Straatheroïne verschilt in sterkte en zuiverheid. Hierdoor kan er een aanzienlijk effect op de symptomen en bijwerkingen bij de gebruiker optreden.Heroïne misbruik en verslaving zijn zeer ernstige medische aandoeningen. Ze vereisen zorg van verslavingsartsen die ervaring hebben met detox en onttrekking van opiaten.
Abstinentie van heroïne op lange termijn kan plotseling ernstige medische complicaties veroorzaken, waaronder de dood. Heroïne detox moet niet thuis worden geprobeerd, of zonder toezicht van een verslavingsarts die regelmatig patiënten behandelt voor Heroïne afhankelijkheid. Als u bij uw dierbare geconfronteerd wordt met een overdosis heroïne of andere opiaten of met ontwenningsverschijnselen, bel 112 voor noodhulp.
Wat zijn de oorzaken van heroïneverslaving?
Heroïneverslaving wordt gekenmerkt door dwangmatig drugs zoeken en gebruiken.Misbruikers melden het gevoel een sterke toename van een aangename gewaarwording die door niets te evenaren is. Deze gewaarwording wordt aangeduide met flash. Deze flash gaat meestal gepaard met warme sensatie van de huid meestal aangeduid als een rush. Blozen in gewoon Nederlands. Verder ervaart de gebruiker een, droge mond, en een zwaar gevoel in de ledematen.
De intensiteit is afhankelijk van de dosis en de snelheid waarmee heroïne in de hersenen komt. Heroïne is bijzonder verslavend omdat het de hersenen zo snel bereikt.
Gebruikers rapporteren hierover dat zij tijdens het begin van het gebruik menen controle te hebben over het gebruik. Pas veel later realiseren zij zich dat zij helemaal geen controle over hun gebruik hebben. Hun hersenen lijken op het gebied van gebruik de controle volledig verloren te hebben. Zij lijken echter ook niet meer een afweging te kunnen maken over hoe groot de impact van hun gebruik is op hun sociale leven. Het sociale leven en ook werk lijkt voor hen niet van belang.
Een ex-gebruiker meldde mij: "Wanneer het zover was gekomen dat ik mijn moeder had moeten verkopen om te kunnen gebruiken, had ik het zonder nadenken gedaan.
In zeker zin is dit gebruikersgedrag van heroïne verslaafden, vergelijkbaar met alcoholgebruikers die menen dat zij zonder problemen een auto kunnen besturen, terwijl ze in nuchtere toestand weten dat drankgebruik gepaard gaat met een slechtere coördinatie. Familie, vrienden of collega's kunnen bij hun dierbare een aantal symptomen en effecten van het gebruik van heroïne waarnemen
| - heroïnegebruik blokkeert het vermogen van de hersenen om pijn waar te nemen. | |
| - Kortademigheid | |
| - Droge mond | |
| - Zeer kleine pupillen | |
| - Plotselinge veranderingen in gedrag. | |
| - Desoriëntatie | |
| - hyper waakzaamheid gevolgd door afwezigheid | |
| - Een neerslachtige houding |
Gedrag dat wijst op heroïne misbruik en verslaving:
| - Het bezit van spullen die dienen voor gebruik, injecteren of consumeren heroïne: Naalden of spuiten die voor andere medische doeleinden, geblakerde zilveren lepels, aluminiumfolie of kauwgom wikkels, ontbrekende schoenveters die gediend hebben om de arm af te binden en zo een geschikte ader voor injecteren te vinden, pijpjes met brandplekken,kleine plastic zakjes, met wit ;poederachtige residu | |
| - Het dragen van een lange broek of lange mouwen om wonden en blauwe plekken van gebruik injectienaalden te verbergen. | |
| - Liegen, verheimelijken tegen ouders, partner, hulpverleners. Tegenover artsen die opiaten voorschrijven wordt het gebruik juist overdreven om meer middelen te verkrijgen. Er wordt veelvuldig op schuldgevoelens ingespeeld. | |
| - Herhaaldelijk stelen of lenen van geld van dierbaren, of onverklaarbare afwezigheid van kostbaarheden | |
| - Toename van schorre onduidelijke, onverstaanbare of onsamenhangende spraak | |
| - Het vermijden van oogcontact, of in de verte staren | |
| - Plotselinge veranderingen in gedrag. | |
| - Een aanzienlijke toename van de tijd doorgebracht in bed | |
| - Afnemende aandacht voor hygiëne en fysieke verschijning | |
| - Vijandig gedrag in de richting van dierbaren, met inbegrip van hen de schuld te geven voor het verlies van of breken met de relatie | |
| - Terugtrekken uit contact met vrienden en familie, in plaats daarvan tijd doorbrengen met nieuwe vrienden met geen natuurlijke band | |
| - Plotselinge verslechtering van de prestaties op school of op het werk, met inbegrip van huisuitzetting en verlies van banen | |
| - Verlies belangstelling voor doelen, hobby's en favoriete activiteiten. | |
| - Reacties die wijzen op verlies van eigenwaarde. |
Gevolgen heroïne gebruik
Gebruikers bouwen tolerantie voor heroïne, wat leidt tot toename van de frequentie en hoeveelheid heroïne. Met de groeiende tolerantie, komen de meer definitieve fysieke symptomen van Heroïne misbruik en verslaving naar voren:| - Gewichtsverlies | |
| - Loopneus | |
| - Naaldsporen, littekens en blauwe plekken zichtbaar armen. | |
| - Infecties en abcessen op de injectieplaats | |
| - Voor vrouwen, het verlies van de menstruele cyclus (amenorroe) | |
| - Snijwonden, kneuzingen en korsten van de huid door kapotkrabben | |
| - hyper waakzaamheid gevolgd door afwezigheid | |
| - Een neerslachtige houding |
Wat zijn de bijwerkingen van heroïneverslaving?
De bijwerkingen zijn niet voor elke gebruiker hetzelfde. De dosering speelt een belangrijke rol. Wanneer er sprake is van afhankelijkheid van een andere chemische substantie beïnvloedt dat ook de presentatie, complicaties en bijwerkingen van heroïnegebruik.Bijwerkingen van Heroïne misbruik en verslaving variëren naarmate de verslaving vordert.
Andere chemische afhankelijkheid kan de presentatie van complicaties en bijwerkingen van Heroïnegebruikbe‹nvloeden.
| - Gezien vereiste nauwkeurige titrering van een dergelijke krachtig verdovend middel als heroïne. Kan er na de flush misselijkheid en overgeven volgen en ernstige jeuk. | |
| - Verzwakte ademhaling (oppervlakkige ademhaling) | |
| - Versuffing. | |
| - sterke jeuk die leidt tot dwangmatig krabben en plukken aan de huid. | |
| - Verminderde pijn van zowel fysieke omstandigheden of emotionele problemen | |
| - Hartproblemen, infectie van het hart, de vaten en kleppen | |
| - Besmettelijke ziektes zoals HIV en Hepatites B en C opgelopen via gedeelde naalden. | |
| - Chronische longontsteking of andere longziekten | |
| - Bloedstolsels of dood weefsel als gevolg van ingestorte aderen of onzuiverheden | |
| - Bacteriële infecties | |
| - Artritis en andere reumatologische problemen | |
| - Epileptische aanvallen | |
| - Omdat Heroïne verslaafden de sterkte en versnijding van de straatheroïne niet kunnen weten, lopen ze het risico van overdosering en zelfs overlijden. |
Ontrekkingsverschijnsel of ontwenningsverschijnselen:
Wanneer de gebruiker geen heroïne tot zijn beschikking heeft of besluit te stoppen met het gebruik, treden onaangename ontwenningsverschijnselen op. Deze ontwenningsverschijnselen zijn zo onaangenaam dat ze een drijvende factor zijn achter veel heroïne recidieven . Bij heroïne verminderen of stoppen beginnen ontwenningsverschijnselen in slechts zes tot 12 uur na de laatste toediening. De ontwenningsverschijnselen bereiken een piek 1-3 dagen na de laatste dosis en verdwijnen na vijf tot zeven dagen .Hoewel ontwenning zelden dodelijk is, kan het ernstige gezondheidsproblemen vormen voor degenen die aan HIV / aids lijden of die zwanger zijn. Typische ontwenningsverschijnselen zijn:
- Ontevreden of onaangename stemming ( dysforie ) .
- Misselijkheid.
- Braken .
-Zweten.
-Kippenvel.
-Verwijde pupillen.
-Spierpijn.
-Verhoogd oogtranen.
-Loopneus.
-Geeuwen.
-Koorts.
-Diarree.
- Slapeloosheid.
-Prikkelbaarheid.
-Verhoogde pijngevoeligheid .
-Spontane zaadlozing.




 Blikkramp is een kramp van de oogspieren waardoor de oogbol naar boven getrokken wordt. Vaak gaat dit gepaard met nekkramp en de persoon wanneer je met hem praat geen oogcontact meer kan maken. Deze vorm van kramp kan zich ook voordoen bij de tong en bij de slik spieren. Dit laatste is zeer ernstig vanwege verslik- en verstikkingsgevaar. De overkoepelende term voor deze vormen van kramp is acute dystonie.
Blikkramp is een kramp van de oogspieren waardoor de oogbol naar boven getrokken wordt. Vaak gaat dit gepaard met nekkramp en de persoon wanneer je met hem praat geen oogcontact meer kan maken. Deze vorm van kramp kan zich ook voordoen bij de tong en bij de slik spieren. Dit laatste is zeer ernstig vanwege verslik- en verstikkingsgevaar. De overkoepelende term voor deze vormen van kramp is acute dystonie.
 Prolactine wordt aangemaakt in de hypofyse. naast prolactine produceert de hypofyse nog 8 andere hormonen. De afgifte van prolactine staat onder controle van de hypothalamus door de remmende werking van dopamine.
Prolactine wordt aangemaakt in de hypofyse. naast prolactine produceert de hypofyse nog 8 andere hormonen. De afgifte van prolactine staat onder controle van de hypothalamus door de remmende werking van dopamine.